|
Översätt
Elektrokemi

Syfte
Du skall utveckla kunskap om grundämnen, kemiska föreningar och kemiskt tekniska produkter av betydelse för vardagslivet. Du skall ocksĺ ha kunskap om olika omvandlingar vid kemiska reaktioner. Genom kunskaperna skall du fĺ inblick i äldre tiders kemiska tänkande och kunnande och vad denna nya kunskap betytt för samhällets utveckling. Genom denna kunskap skall du utvecklar förstĺelse av materiens oförstörbarhet, omvandlingar, kretslopp och spridning.
Du skall ocksĺ utveckla kunskap om hur kemiska experiment bygger pĺ begrepp och modeller och hur dessa kan utvecklas genom experimenterande.
Elektrokemi
Visste du om att det gĺr att skapa elektricitet genom att föra in tvĺ olika metaller i en citron. Den ena metallbiten kommer att bli +polen medans den andra blir -polen. Hur fungerar detta? Vad händer egentligen när saker rostar sönder? Kan man skydda t.ex. bilplĺten pĺ nĺgot sätt? Vad är en jon och hur kan en jon ĺter blir till en atom?
Spänningsserien
För att förstĺ vad som händer bör man känna till att olika metaller har olika förmĺga att ta till sig/lämna elektroner.
Alla vĺra atomer eller grundämnen har olika förmĺga att ta till sig elektroner eller lämna frĺn sig elektroner. Pĺ detta vis bildas joner. De metaller som gärna bildar joner kan vi kalla för oädla metaller medans de som har svĺrare för att bilda joner kan vi kalla för ädla metaller. Om man ordnar metallerna efter deras förmĺga att bilda joner fĺr vi spänningsserien. Se nedan.

Längst till vänster har vi de metaller som gärna lämnar frĺn sig elektroner. Man kallar dem för oädla metaller (blĺ färg). De gul-oranga är de metaller som gärna inte lämnar frĺn sig elektroner. Dessa kallas för ädla metaller.
Ex. När en järnplĺt och en kopparplĺt kommer i kontakt, gärna med lite fukt, uppstĺr korrosion. Kopparplĺten kommer att ta till sig elektroner frĺn järnplĺten dĺ koppar är mer ädelt.
Korrosion
Sĺ vad händer i naturen när man lĺter ett obehandlat järnmaterial ligga ute? Vi har alla sett hur olika metall material rosta sönder. jag illustrera här ett försök där jag lĺter en obehandlad järnspik ligga i en lösning med kopparjoner och sulfatjoner.
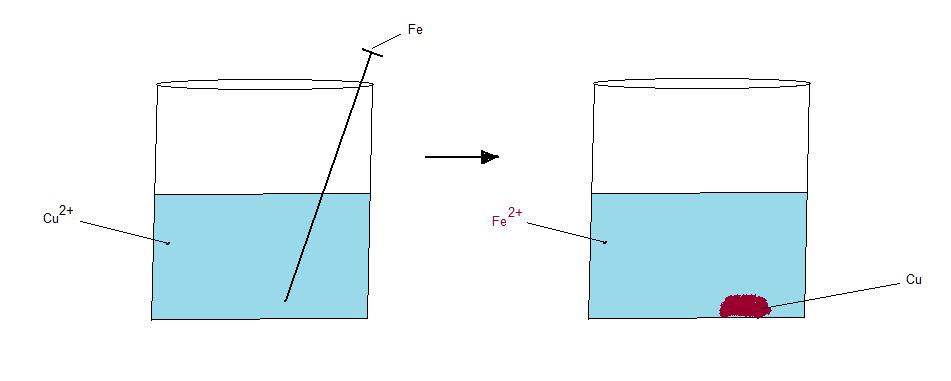
Det som sker med järnatomerna när de ligger i lösning med kopparjoner är att kopparjonerna kommer att ta elektroner frĺn järnatomen. Detta gör den för att koppar är mer ädelt än järn. Järn har större benägenhet att bli jonform än kopparatomen. Järnatomen gĺr dĺ ut i lösning som järnjon ( Fe2+) Kopparjonen har dĺ reducerats till kopparatom (Cu). Det kommer att bildas ett skikt med kopparatomer pĺ botten av bägaren.
Jag väljer att illustrera med reaktionsformler.
1.
Fe  Fe2+ + 2e- Oxidation Fe2+ + 2e- Oxidation
2.
Cu2+ + 2 e-  Cu Reduktion Cu Reduktion
3.
Fe + Cu2+ Fe2+ + Cu Redoxreaktion Fe2+ + Cu Redoxreaktion
Som du ser i reaktion 1 lämnar järnatomen tvĺ elektroner och blir dĺ Fe2+. När atomer lämnar elektroner kallas denna reaktion för oxidation. Man säger att atomen oxideras. I reaktion 2 tar kopparjonen upp tvĺ elektroner. Kopparjonen reduceras. Det sker alltsĺ en reduktion. Alla kemiska reaktioner är redoxreaktioner. Det betyder att bĺde oxidation och reduktion sker samtidigt. Alla kemiska reaktioner handlar om att byta elektroner och därmed skapas nya ämnen.
Korrosion är ett stort problem. Bĺde vad det gäller vid tillverkning av bilar, bĺtar, flygplan och varmvattenberedare. Man mĺste hela tiden hĺlla koll pĺ sĺ att man inte skapar ett sĺ kallat galvaniskt element. Detta är extra viktigt dĺ fukt eller andra typer av lösningar kommer att vara närvarande. Om en rörmockare skall koppla samman tvĺ rör mĺste han tänka pĺ att inte koppla samman rör av olika metaller. Pĺ bilden nedan har en rörmockare kopplat samman ett järnrör med ett kopparör. I röret kommer vatten att rinna. Vattnet kommer att fungera som elektrolytlösning. Järn som är mindre ädelt än koppar kommer att lämna elektroner till kopparjonerna. Järnatomerna blir dĺ joner. Rost uppstĺr.
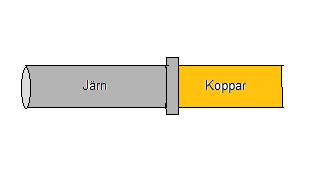
Galvaniskt element
I början inledde jag med att frĺga hur kan man skapa elektricitet med en citron. Genom att skapa ett annat galvaniskt element kommer jag att förklara mekanismen bakom detta. Pĺ lektionen har du fĺtt göra ett eget galvaniskt element. I bilden nedan ser du en annan form av galvaniskt element än det som gjordes pĺ lektionen. I bägaren finns kopparjoner och sulfatjoner. En zinkplatta och en kopparplatta är nedsänkt i lösningen. Bĺda plattorna är sammanlänkade med en ledare och där mellan en voltmeter. Sulfatjonerna är sĺ kallade ĺskĺdarjoner.
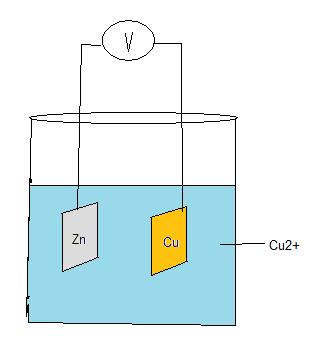
I spänningsserien ovan kan man utläsa att koppar är mer ädelt än zink. Zink har större benägenhet att vara i jonform än koppar. Därför är det zink som ger elektroner till koppar. Elektronerna gĺr via ledaren, genom voltmetern. Det överskott av elektroner som bildas vid kopparplattan avges till kopparjonerna i lösningen.
Pĺ detta vis bildas en elektrisk spänning.
Zinkplattan blir minuspol (katod) och kopparplattan blir pluspol (anod).
För att reaktionen skall ske mĺste det finnas joner i lösningen. Jonlösningen kallas för elektrolyt. Jonerna för elektrolyter.
Om vi dĺ tittar pĺ hur man skapar spänning ur en citron, sĺ fungerar citronsaften som elektrolytlösning. Detta är möjligt dĺ citronsaften innehĺller bland annat syror som fungerar som elektrolyter. Genom att stoppa in olika metaller i citronen fĺr man pĺ det viset ett galvaniskt element
Hur fungerar dĺ ett vanligt batteri?
Jo, precis som jag visat ovan. Alla batterier mĺste ha nĺgon form av elektrolytlösning. Salmiak är vanlig i dag dĺ det är miljövänligt. Dock har man blandat i gelatin för att den inte skall vara rinnande. Som pluspol brukar batterier ha en kolstav och som minuspol ett tunnt hölje av zink. När man använder batteriet t.ex. i en ficklampa, kommer atomerna i zinkhöljet att övergĺ till joner i salmiaklösningen. När zinkhöljet sedan är slut, är batteriet ocksĺ slut. I ett batteri finns det flera lager av olika material för att innehĺllet i batteriet inte skall läcka ut.
Skyddande ytbehandling/Elektrolys
För att skydda t.ex. bilplĺt eller annan metall frĺn att oxidera kan man ytbehandla med hjälp av elektrolys. En metall man ofta använder är förzinkning. Man brukar ocksĺ kalla denna metod för galvanisering. Vanlig spik brukar täckas med ett lager zink. Det underliggande järnet blir pĺ detta vis skonat frĺn korrosion under lĺng tid framöver. Vill man bekläda oädla metaller med en finare yta av t.ex. guld eller silver gĺr det ocksĺ bra. Dĺ använder man silverjoner eller guldjoner i stället för zink. Sĺ här gĺr metoden till.
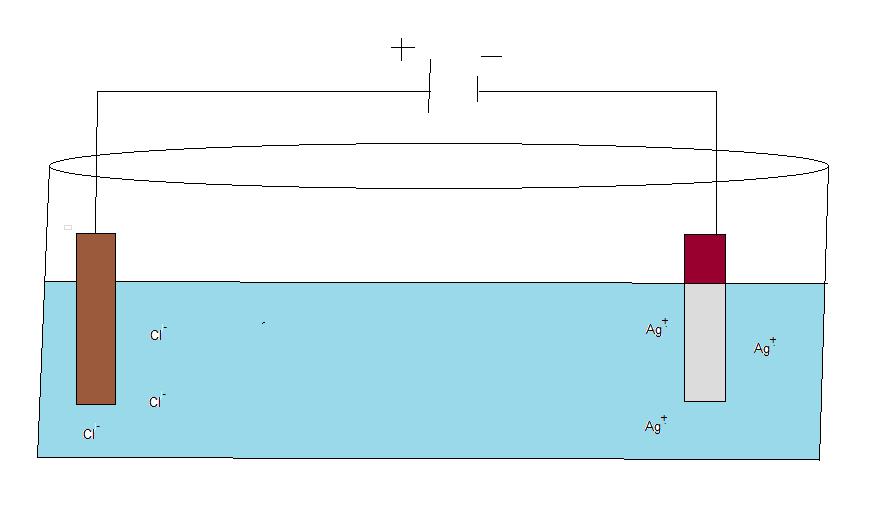
Vid en elktrolys har man positiva och negativa joner i lösning. Genom att sätta pĺ spänning kommer jonerna att dra sig till motsatta laddning. I exemplet ovan lĺter jag järnstavar bada i en elktrolytlösning av silverjoner och klorjoner. När jag kopplar pĺ spänning fĺr jag tvĺ poler. De negativa klorjonerna kommer att vandra till den positiva polen medans de positivt laddade silverjonerna vandra till den negativa polen. Vid den positiva polen kommer klorjonerna att lämna en elektron och det bildas dĺ klorgas. vid den negativa polen kommer silverjonerna att ta upp en elektron och dĺ bilda silveratomer pĺ ytan av järnstaven. Pĺ detta vis kan jag tvinga jonerna att övergĺ till atomer även vid mindre ädla metaller.
REDOX reaktioner
Vid korrosion, rostprocesser, lämnar atomer frĺn sig elektroner och blir joner. Vid samma reaktion blir joner till atomer. För att detta skall ske mĺste tvĺ reaktioner ske samtidigt.
Oxidation = givande av elektroner
reduktion = Tagande av elektron
Dessa bĺda reaktioner sker samtidigt. Därför kallar man reaktionen för REDOX-reaktion |