|
Studieuppgifter

Atom och kõrnfysik
Begrepp att kõnna till och kunna anvõnda i dina diskussioner
- Subatomõra partiklar protoner, neutroner och elektroner
- Masstal
- Atomnummer
- GrundtillstÕnd
- Exiterat tillstÕnd
- Kontinuerligt spektrum
- Linjespektrum
- Absorbtionsspektrum
- Elektromagnetiska vÕgor
- R÷ntgen
- Radioaktivitet
. Alfa, beta och gammastrÕlning
- Deuterium (võteisotop)
- Tritium (võteisotop)
- Halveringstid
- Enheter f÷r s÷nderfall becquerel
- Fission
- Fusion
Atomen
Nõr man ritar en atom anvõnder vi en modell som kallas f÷r planetmodellen. Det var den danske fysiken Niels Bohr som kom pÕ iden till denna atommodell. I Bohrs modell finns tre subatomõra partiklar, protoner, neutroner och elektroner. F÷r att atomen skall vara neutral, alltsÕ ingen laddning, finns lika mÕnga protoner (+) som elektroner (-).
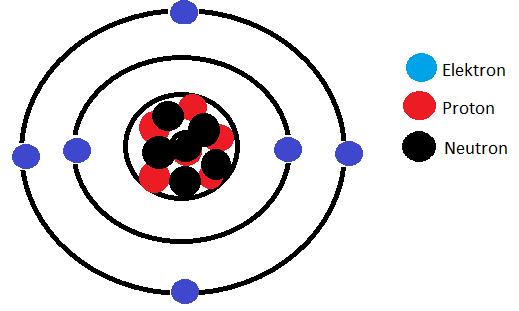
Detta õr en kolatom. Den õr uppbygd av 6 protoner, 6 neutroner och 6 elektroner
Atomnummer
I en atom õr det protonen och neutronen som võger, har massa. Elektronen har i stort sett ingen massa om man jõmf÷r med protoner och neutroner. Atomnumret sõger hur mÕnga protoner det finns i en atomkõrna. PÕ detta vis vet du ocksÕ hur mÕnga elektroner det finns runt kõrnan eftersom atomen saknar leddning.
13Al Aluminium har atomnummer tretton.
Masstal
Masstalet anger hur mÕnga protoner och neutroner det finns i atomkõrnan. Genom att subtrahera atomnumret med masstalet fÕr du fram antalet neutroner i kõrnan. Masstalet õr siffran som õr upph÷jd framf÷r det kemiska tecknet. Kol har atomnummer 6 och masstalet 12.

GrundtillstÕnd
Elektronerna befinner sig i sina elektronbanor. Beroende pÕ vilken energi elektronen har, har de lika avstÕnd till atomkõrnan, de befinner sig i olika skal beroende pÕ vilken energi elektronerna har. En atom som har sina elektroner i sina ordinarie, vanliga, banor sõgs befinna sig i sitt grundtillstÕnd.
Exciterat tillstÕnd
Elektronerna i kan ta upp energi frÕn omgivningen. Detta utnyttja man i bland annat lysr÷r. I lysr÷ret finns argongas och f÷rÕngad kvicksilver. Nõr man lÕter str÷m passera genom gasen tar elektronerna upp energin. Elektronerna fÕr dÕ h÷gre energi. Elektronerna hoppar dÕ ut till en elektronbana lõngre ut. Detta tillstÕnd kallas exciterat tillstÕnd. en exciterad atom kan õr mycket reaktiv och behÕller tillstÕndet en brÕkdels sekund.
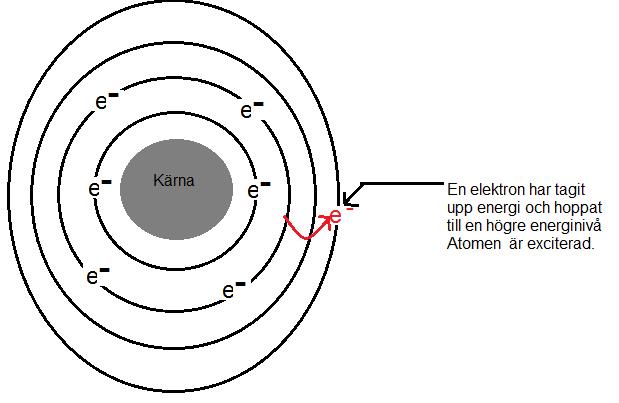
Nõr elektronen inte lõngre kan behÕlla energin slõpper den energin i form av en partikel som kallas f÷r foton eller ljusblixt. samtidigt som den slõpper energin faller den tillbaka till sin normala elektronbana, alltsÕ till sitt grundtillstÕnd. Att vi ser konstant ljus frÕn ett lysr÷r beror pÕ att miljarder och Õter miljarder av exciterade atomer ger upphov till ett ljus som vi upplever konstant och inte som ljusblixtar.
Spektrum
Ett spektrum skall ses som en uppdelning av elektromagnetiska vÕgor. PÕ detta vis kan man fÕ ljuset att dela upp sig i regnbÕgens alla fõrger.

Bild frÕn wikipedia
Ljus frÕn solen har vÕglõngder frÕn alla fõrger som mõnniskan kan se. DÕ ljuset delar upp sig nõr den passerar en prisma kan man se all fõrgerna i spektret. Detta spektra kallas f÷r kontinuerligt spektra. Ljus med alla fõrgerna upplevs av mõnniskan som vitt ljus.
Om ljus med kontinuerligt spektra fÕr passera en gas och sedan passera en prisma uppstÕr ett absorptionsspektra. Vissa fõrger har absorberats och dõrf÷r framtrõder inte alla fõrger. PÕ de platser dõr de absorberade fõrgerna skulle varit finns nu m÷rka strõck.

Om en upphettad gas ger frÕn sig ljus med ett fÕtal vÕglõngder fÕr man emissionsspektrum. endast ett fÕtal vÕglõngder avges. I spektret uppstÕr emissionslinjer i de fõrger som varje vÕglõngd stÕr f÷r.

Elektromagnetiska vÕgor
Elektromagnetska vÕgor õr en vÕgr÷relse. Beroende pÕ vilken vÕglõngd den elektromagnetiska vÕgorna har kallas de olika.
Namn VÕglõngd
RadiovÕgor ųver en meter
MikrovÕgor Ca 1mm-1m
Infrar÷d strÕlning mindre õn 0,1mm
Synligt ljus 400-800nm
Ultraviolett 100-1nm
R÷ntgen 0,01nm
GammastrÕlning 0,001nm
R÷ntgen
Wilhelm R÷ntgen fick 1895 nobelpriset f÷r sin upptõckt om r÷ntgenstrÕlarna. Det han kom pÕ var att elektromagnetisk strÕlning gÕr igenom kroppens mjuka võvnader men inte benen. PÕ detta vis kunde man se om nÕgot var brutet.
Radioaktivitet
Viktiga personer att kõnna till õr Henri Becquerel samt Marie och Pierre Curie. Henri kom pÕ att atomkõrnorna faller s÷nder och sõnder ut strÕlning. Marie och Pierre kom pÕ grundõmnet radium som utsõnder mycket starkare strÕlning õn uran.
En atomkõrna som inte õr stabil faller s÷nder och avger olika typer av radioaktivitet. Nedan faller uran 238 s÷nder till en heliumkõrna och en toriumkõrna. AlfastrÕlning bestÕr alltsÕ av heliumkõrnor. ─ven om alfastrÕlning õr farligt nÕr den inte speciellt lÕngt, den stoppas av ett tunt papper.

BetastrÕlning bestÕr av elektroner. Denna strÕlning nÕr lõngre och õr svÕrare att stoppa. Dock rõcker en tjockare trõbit. Elektronerna kommer frÕn kõrnan. Detta õr m÷jligt dÕ neutronen õr uppbyggd av en proton och en elektron.
GammastrÕlning õr inte materia utan elektromagnetisk strÕlning. Denna strÕlning õr joniserande vilket betyder att den ger joner. Joner i sin tur kan orsaka cancer. alfa och betastrÕlning õr ocksÕ joniserande.
Isotoper
Võte õr vÕrt minsta grundõmne. Vanligen bestÕr den av en proton i kõrnan och en elektron som cirkulera runt kõrnan. Det finns andra typer av võte. Dessa kallas f÷r isotoper. Võtets isotoper har neutroner i kõrnan. Deuterium har en neutron i võtekõrnan. Tritium har tvÕ neutroner i võtekõrnan. BÕde tritium och deuterium õr tyngre õn vanligt võte. Om en vattenmolekyl õr uppbyggt av deuterium eller tritium istõllet f÷r vanligt võte kallas det f÷r tungt vatten.

Tillbaka
|